L’insufficienza cardiaca con frazione di eiezione ridotta (HFrEF) è un tipo importante di insufficienza cardiaca e il China HF Study ha dimostrato che il 42% degli scompensi cardiaci in Cina sono HFrEF, sebbene siano disponibili diverse classi terapeutiche standard di farmaci per HFrEF e abbiano ridotto il rischio di morte e di ospedalizzazione per insufficienza cardiaca in una certa misura. Tuttavia, i pazienti sono ad alto rischio di eventi ricorrenti di peggioramento dell’insufficienza cardiaca, la mortalità rimane intorno al 25% e la prognosi rimane sfavorevole. Pertanto, c'è ancora un urgente bisogno di nuovi agenti terapeutici nel trattamento dell'HFrEF e Vericiguat, un nuovo stimolatore della guanilato ciclasi solubile (sGC), è stato studiato nello studio VICTORIA per valutare se Vericiguat potrebbe migliorare la prognosi dei pazienti con HFrEF. Lo studio è uno studio sugli esiti clinici di fase III, multicentrico, randomizzato, a gruppi paralleli, controllato con placebo, in doppio cieco, basato sugli eventi. Condotto sotto gli auspici del VIGOR Centre in Canada in collaborazione con il Duke Clinical Research Institute, hanno partecipato allo studio 616 centri in 42 paesi e regioni, tra cui Europa, Giappone, Cina e Stati Uniti. Il nostro reparto di cardiologia è stato onorato di partecipare. Un totale di 5.050 pazienti con insufficienza cardiaca cronica di età ≥18 anni, classe NYHA II-IV, EF <45%, con livelli elevati di peptide natriuretico (NT-proBNP) entro 30 giorni prima della randomizzazione e che erano stati ricoverati in ospedale per insufficienza cardiaca sono stati arruolati nello studio entro 6 mesi prima della randomizzazione o avevano ricevuto diuretici somministrati per via endovenosa per insufficienza cardiaca entro 3 mesi prima della randomizzazione, tutti ricevevano ESC, AHA/ACC e nazionali/regionali linee guida specifiche raccomandano standard di cura. I pazienti sono stati randomizzati in un rapporto 1:1 in due gruppi e sono stati somministratiVericiguat(n=2526) e placebo (n=2524) in aggiunta alla terapia standard, rispettivamente.
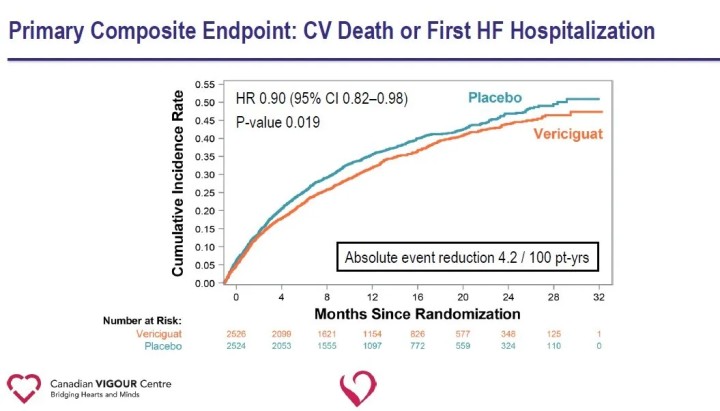
L'endpoint primario dello studio era l'endpoint composito di morte cardiovascolare o primo ricovero per insufficienza cardiaca; gli endpoint secondari includevano componenti dell'endpoint primario, il primo e i successivi ricoveri per insufficienza cardiaca (primi eventi ed eventi ricorrenti), l'endpoint composito di morte per tutte le cause o ospedalizzazione per insufficienza cardiaca e morte per tutte le cause. Ad un follow-up mediano di 10,8 mesi, è stata osservata una riduzione relativa del 10% dell’endpoint primario di morte cardiovascolare o primo ricovero per insufficienza cardiaca nel gruppo Vericiguat rispetto al gruppo placebo.
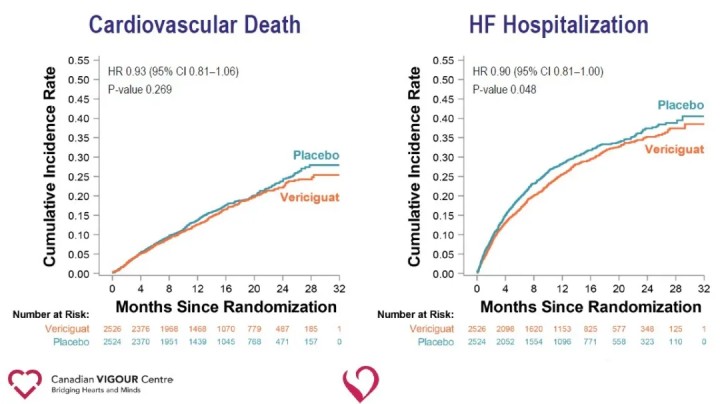
L'analisi degli endpoint secondari ha mostrato una riduzione significativa del ricovero per insufficienza cardiaca (HR 0,90) e una riduzione significativa dell'endpoint composito di morte per tutte le cause o ricovero per insufficienza cardiaca (HR 0,90) nel gruppo Vericiguat rispetto al gruppo placebo.
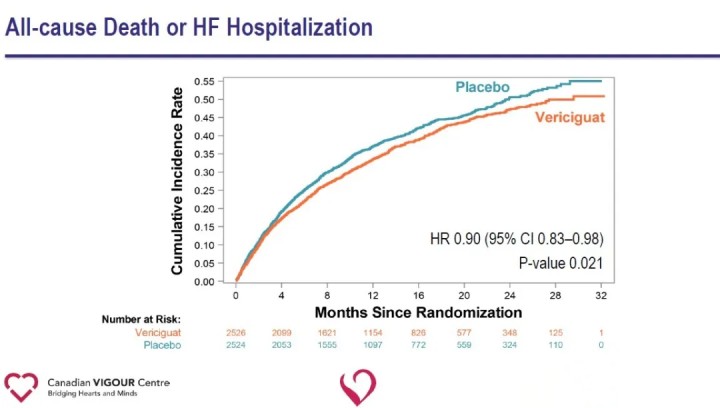
I risultati dello studio suggeriscono che l'aggiunta diVericiguatal trattamento standard dell’insufficienza cardiaca riduce significativamente il recente verificarsi di peggioramento degli eventi di insufficienza cardiaca e riduce il rischio dell’endpoint composito di morte cardiovascolare o ospedalizzazione per insufficienza cardiaca nei pazienti con HFrEF. La capacità di Vericiguat di ridurre il rischio dell’endpoint composito di morte cardiovascolare o ospedalizzazione per insufficienza cardiaca in pazienti con insufficienza cardiaca ad alto rischio fornisce una nuova strada terapeutica per l’insufficienza cardiaca e apre nuove strade per la futura esplorazione delle malattie cardiovascolari. Vericiguat non è attualmente approvato per la commercializzazione. La sicurezza, l’efficacia e il rapporto costo-efficacia del farmaco devono ancora essere ulteriormente testati sul mercato.
Orario di pubblicazione: 09-febbraio-2022
